Com prazo até 2016 para se adequarem ao projeto de rastreabilidade de medicamentos (Lei 11.903, de 2009), o setor de saúde deve movimentar mais de R$ 4 bilhões, principalmente nos setores de Tecnologia da Informação (TI), de Automação e Logística
A previsão é dos organizadores do Seminário de Tecnologia de Rastreabilidade de Medicamentos (SETRM), que será realizado no dia 27 de maio, em São Paulo, no Auditório do Instituto de Radiologia (INRAD) da Universidade de São Paulo (USP).
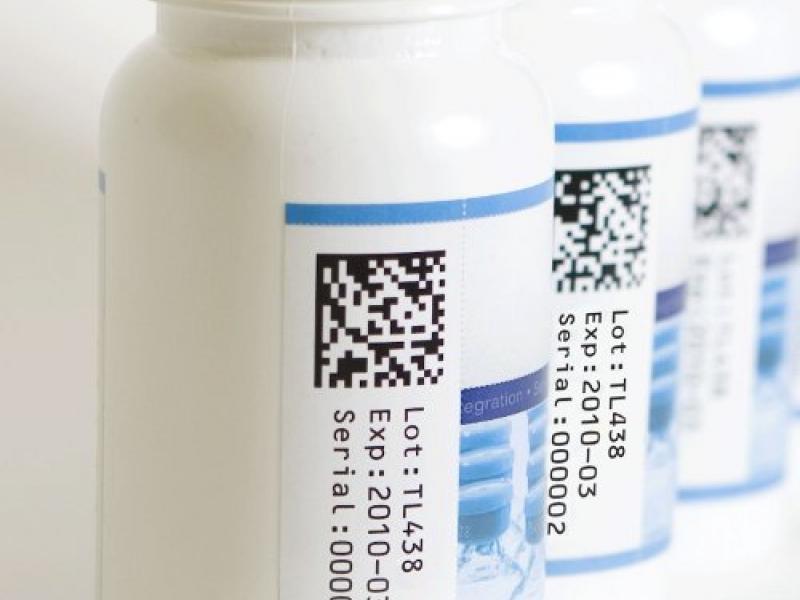
Com o intuito de proteger a segurança do paciente, assim como inibir falsificação de remédios entre outras irregularidades, a nova legislação criou o Sistema Nacional de Controle de Medicamentos (SNCM), que determina que cada produto farmacêutico passe a ter um RG, viabilizando que, em qualquer etapa da cadeia, possa ser verificada a autenticidade do remédio.
O Sindusfarma (Sindicato da Indústria Farmacêutica) estima que só na produção de medicamentos serão necessários investimentos superiores a R$ 1 bilhão, distribuídos entre 2014 e 2016. A estratégia do Brasil foi executar o projeto em duas fases, a primeira de implantação, com início em 2013 até este ano, e a segunda em dezembro de 2016.
Números
- 100 mil pessoas foi a média anual de mortes por uso de medicamentos ilegais de 2000 a 2007
- US$ 75 bilhões foi a movimentação de remédios falsificados em 2010 em todo o mundo
- R$ 2,5 bilhões é a perda anual de arrecadação com medicamentos contrabandeados no Brasil
- 20% dos medicamentos consumidos no Brasil são ilegais, contra 10% da média mundial
- 50% dos medicamentos comercializados na internet são pirateado
- 800 % foi o crescimento que a venda de medicamentos ilegais apresentou no período de 2000 a 2007
- 1º entre os 10 produtos mais pirateados, como fonte de lucro para os contrabandistas
Experiência fora
Os Estados Unidos é exemplo de uma implementação desse tipo em um curto espaço de tempo, sendo 10 vezes maior do que o brasileiro, de acordo com o IMS Health, e é altamente complexo, com quase 200 mil fabricantes, distribuidores, farmacêuticos, hospitais, clínicas e escritórios médicos na cadeia de suprimentos.
Os Estados Unidos é exemplo de uma implementação desse tipo em um curto espaço de tempo, sendo 10 vezes maior do que o brasileiro, de acordo com o IMS Health, e é altamente complexo, com quase 200 mil fabricantes, distribuidores, farmacêuticos, hospitais, clínicas e escritórios médicos na cadeia de suprimentos.
“Quando a lei americana foi sancionada, a indústria tinha apenas 13 meses para atender à primeira fase da regulamentação, e a lei não definia como a indústria deveria fazer o intercâmbio exigido de informações de rastreabilidade através da cadeia de suprimentos”, disse Brian Daleiden, vice-presidente de Marketing da TraceLink, empresa provedora de soluções de rastreabilidade, em nota ao mercado. “Os líderes da indústria, os associados à indústria e os provedores de tecnologia rapidamente se juntaram para negociar suas diferenças e definir um tipo de padrão que se aproximasse às exigências de troca de informações a tempo do prazo de 1° de janeiro de 2015”, completou Daleiden.
Uma das empresas pioneiras no comprometimento com o projeto foi a Libbs, que afirma já colher ganhos indiretos em termos de eficiência operacional, o que deve reduzir o custo dos medicamentos para todo o sistema. “O grande vencedor da implementação, em um futuro próximo, será o consumidor, que terá, através da rastreabilidade, possibilidades de verificar a procedência do medicamento”, disse o Amilcar Lopes, CEO da R&B Rastreabilidade Brasil, responsável pela implantação da Libbs.

Adiamento
No início deste mês foi apresentado o projeto de Lei Nº 276, de 2015 (de autoria do senador Humberto Costa – PT), que se adianta propondo uma mudança da Lei 11.903, antes que os resultados da fase piloto sejam apurados. Para o Prof. Dr. Giovanni Guido Cerri, presidente do Conselho Diretor do Instituto de Radiologia do HCFMUSP, se a PL for aprovada, “seria um atraso injustificado. A implantação da rastreabilidade precisa ocorrer em conformidade com a complexidade da cadeia brasileira e com o nível de gravidade local da ilegalidade”.
No início deste mês foi apresentado o projeto de Lei Nº 276, de 2015 (de autoria do senador Humberto Costa – PT), que se adianta propondo uma mudança da Lei 11.903, antes que os resultados da fase piloto sejam apurados. Para o Prof. Dr. Giovanni Guido Cerri, presidente do Conselho Diretor do Instituto de Radiologia do HCFMUSP, se a PL for aprovada, “seria um atraso injustificado. A implantação da rastreabilidade precisa ocorrer em conformidade com a complexidade da cadeia brasileira e com o nível de gravidade local da ilegalidade”.
Saúde Web

Nenhum comentário:
Postar um comentário