 |
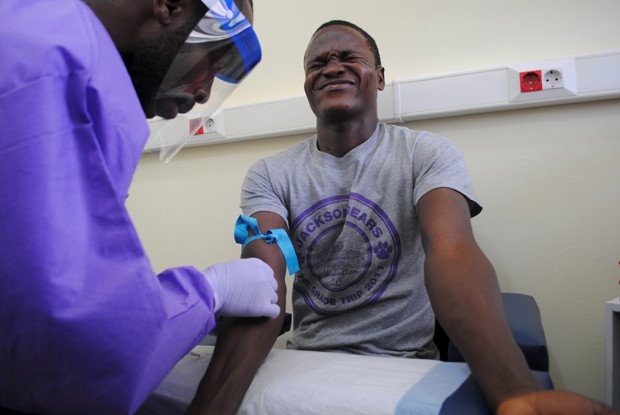
| Foto: Reuters/Stringer - Sobrevivente do ebola tem sangue retirado para estudo em Monróvia, na Libéria |
Qualquer pessoa que contrair gripe aviária neste inverno na Europa pode ser convidado a participar de um teste clínico no qual receberá uma droga (que pode funcionar ou não) ou então paracetamol e um aconselhamento padrão para repouso.
Aqueles que concordarem poderão ajudar o mundo a se preparar para a próxima pandemia potencialmente mortal, bem como ajudar cientistas que estão desesperados para preencher lacunas no conhecimento deixadas por oportunidades perdidas anteriormente.
Cientistas estão desorientados sobre como parar ou tratar a onda de problemas globais nunca vistos nos anos recentes. Entre as preocupações estão doenças como o vírus da MERS (síndrome respiratória do Oriente Médio), uma nova linhagem morta de gripe aviária na China e um surto de ebola sem precedentes no oeste da África.
Eles nem sequer foram capazes de determinar com precisão de onde elas vieram.
O problema é que estudos vitais para analisar as rotas de transmissão e testar drogas e vacinas experimentais simplesmente não foram feitos durante as epidemias, afirmam infectologistas.
É uma falha da ciência, e algo que não deveria acontecer de novo, afirmam.
 |
| Foto: Kim Hong-ji/Reuters - Turistas usam máscaras como prevenção contra a MERS em Seul, Coreia do Sul |
"Não temos uma vacina para a SARS [síndrome respiratória aguda grave] se ela voltar amanhã; não sabemos como tratar a MERS; levamos de seis a nove meses para começar testes clínicos de vacinas para ebola enquanto quase 12 mil pessoas morreram; e durante a pandemia de H1N1 o número de pessoas em estudos clínicos randomizados foi perto de zero."
Burocracia bizantina
A burocracia, a logística e a falta de planejamento antecipado estão no cerne do problema, afirma Trudie Lang, professora de pesquisa em saúde global na Universidade de Oxford, que tem estudo maneiras de reduzir esses obstáculos.
A burocracia, a logística e a falta de planejamento antecipado estão no cerne do problema, afirma Trudie Lang, professora de pesquisa em saúde global na Universidade de Oxford, que tem estudo maneiras de reduzir esses obstáculos.
Durante o surto de ebola que varreu a Guiné, a Libéria e Serra Leoa, a equipe de Lang, especializada em planejar e executar testes em populações frágeis em condições difíceis, foi encarregada de montar um estudo clínico para um tratamento potencial contra ebola chamado brincidofovir.
"Normalmente, leva-se 18 meses para organizar um teste, e nós fizemos em 16 semanas", conta a pesquisadora. "Mas o problema é que nós ainda estávamos abaixo da curva."
Na pandemia de 2009 do vírus H1N1, a "gripe suína", muitos governos estocaram drogas antivirais como o Tamiflu, da Roche, e o Relenza, da GSK. Médicos as prescreviam como medida preventiva sem diagnósticos confirmados, e nenhum teste clínico randomizado foi conduzido para saber se elas ajudaram.
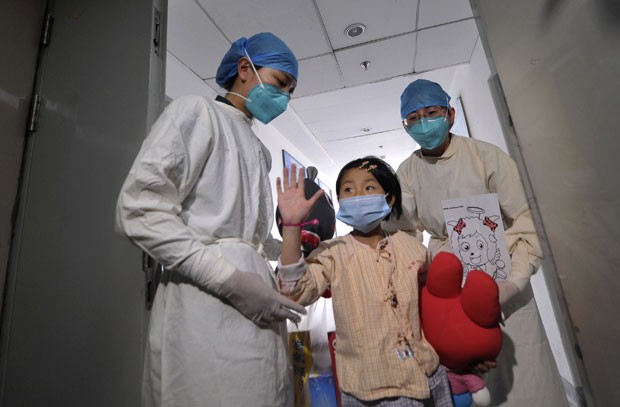 |
| Foto: Divulgação/Reuters - Garota chinesa que foi infectada pelo vírus H7N9 sobreviveu em Pequim |
"É lamentável que não tenhamos aproveitado ao máximo nossa oportunidade para gerar evidências", afirma Chris Butler, professor de clínica na Universidade de Cardiff que está trabalhando agora em um teste sobre gripe em toda a Europa e espera conseguir preencher a lacuna das evidências.
Não há dúvida de que lançar testes clínicos em uma epidemia é algo difícil parcialmente porque linhagens de doenças novas e raras e infectam muitas pessoas, sobrecarregando serviços de saúde.
Mas parte do problema são os entraves burocráticos.
A equipe de Lang recebeu verbas em setembro de 2014, e em janeiro de 2015 conseguiu começar os testes, mas isso coincidiu com uma queda acentuado no número de pacientes de ebola, com a epidemia no oeste da África atingindo um platô.
Cientistas relatam volumes brutais de preenchimento de formulários, fazendo "x" em quadradinhos, reuniões de comitês e assinaturas de acordos envolvidos na realização de um teste clínico.
"Há uma grande indústria interessada em fazer profissionais de testes clínicos passarem por um calvário", afirma Butler. "Há uma miríade de permissões necessárias, é um processo bizantino que pode levar meses."
"Me dá dor de cabeça só pensar em todas as aprovações necessárias", incluindo as de comitês de ética, patrocinadores, advogados, chefes de pesquisa e desenvolvimento e clínicos, afirmou.
Acordos legais são necessários entre fornecedores do produto -- a droga ou vacina experimental ou outra intervenção -- e as pessoas conduzindo o teste, os patrocinadores e hospitais, clínicas ou centros de saúde onde os pacientes serão recrutados.
Em um cenário de epidemia de doença infecciosa, particularmente em uma rápida como a gripe ou o ebola, esses problemas legais podem ocorrer junto de uma competição pelo acesso aos pacientes.
Durante a epidemia de ebola, por exemplo, havia cinco ou seis diferentes grupos de pesquisa tentando organizar e conduzir testes nos três países mais afetados, todos eles com sistemas de saúde limitados pela sobrecarga de pacientes e devastados pela epidemia.
"Foi patético, porque nós essencialmente tivemos de brigar pelos mesmos pacientes", disse ela. "Foi como uma disputa de terreno, e na época os novos casos já estavam diminuindo."
Planejando com antecedência
Aquilo que não se conhece é parte da ameaça de qualquer epidemia, seja o ebola na África, o surto de SARS em 2003, a MERS na Arábia Saudita ou a nova gripe aviária H7N9 na China.
Aquilo que não se conhece é parte da ameaça de qualquer epidemia, seja o ebola na África, o surto de SARS em 2003, a MERS na Arábia Saudita ou a nova gripe aviária H7N9 na China.
Ainda assim, Lang e outros afirmam que não há nada impedindo que os tipos de testes clínicos em uma epidemia não possam ser e sua maior parte discutidos, planejados, assinados e confirmados por antecedência.
"Precisamos ter protocolos prontos para partida", afirma ela. "Precisamos ter uma força-tarefa de equipes de pesquisa em cada região em alerta para ser recrutada em testes durante os próximos surtos."
Contratos legais, por exemplo, cobrem geralmente as mesmas coisas para cada teste -- compartilhamento e armazenamento de dados, confidencialidade de pacientes, consenso informado, etapa de publicação dos resultados, além de preço produção e disponibilidade dos produtos quando eles se mostram úteis.
E em uma epidemia que se espalha velozmente, que pode ser impactante demais para permitir meses de organização, uma abordagem coordenada poderia superar o problema de ter múltiplos grupos de pesquisa sem pacientes o suficiente.
Segundo Lang, isso seria preferível do ponto de vista ético e científico. Quando um teste clínico tem de ser cancelado por sofrer falta de participantes com a doença em questão, isso significa que aquelas pessoas correram riscos em vão.
"O principal problema é que isso precisa ser feito em dias, em vez de semanas ou meses", ela afirma.
"Isso basicamente significa que a pesquisa precisa estar embutida na reação inicial a uma epidemia, e não como uma reflexão tardia."
"Isso basicamente significa que a pesquisa precisa estar embutida na reação inicial a uma epidemia, e não como uma reflexão tardia."
G1

Nenhum comentário:
Postar um comentário