Psiquiatras, neurocirurgiões e neurologistas poderão prescrever o canabidiol como medicamento para crianças e adolescentes com epilepsia, ou que sofram convulsões
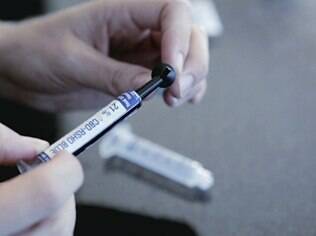 |
| Canabidiol: remédio extraído da maconha poderá ser usado por crianças epiléticas |
O Conselho Federal de Medicina (CFM) decidiu autorizar neurocirurgiões, neurologistas e psiquiatras a prescreverem remédios à base de canabidiol CBD) para crianças e adolescentes portadores de epilepsias cujos tratamentos convencionais não surtiram efeito. O texto da nova regulamentação foi encaminhado nesta quinta (11) para publicação no Diário Oficial da União e a medida entra em vigor nos próximos dias, quando for publicada.
A importação do produto, que não é fabricado no Brasil, só pode ser feita com autorização da Agência Nacional de Vigilância Sanitária (Anvisa). Ainda assim, a iniciativa do conselho é classificada como um avanço na luta pela liberação deste tipo de medicamento, já que para obter o aval da agência, pacientes e parentes de quem usa, ou quer utilizar o canabidiol, precisam apresentar receita e laudo médico, além de termo de responsabilidade e formulário de solicitação de importação para remédios controlados. Muitos médicos se negavam a fornecer a receita e assinar o termo de responsabilidade conjunta por temerem sanções administrativas, já que a prática não era regulamentada pelo CFM.
Leia também:
Leia também:
Anvisa divulga como importar remédio com substância controlada
Confira como importar medicamentos controlados e sem registro no Brasil
Grupo desafia a lei para produzir remédio extraído da maconha
A Resolução CFM nº 2113 proíbe a prescrição da Cannabis sativa (nome científico da maconha)in natura para uso medicinal, bem como de quaisquer outros derivados da planta que não o canabidiol, empregado exclusivamente com fins terapêuticos. O texto também estabelece as dosagens recomendadas e a forma de monitoramento dos resultados alcançados a partir da prescrição. O grau de pureza da substância e sua forma de apresentação deverão seguir as determinações da Anvisa.
O CFM garante ter aprovado a prescrição após avaliar todos os fatores relacionados à segurança do paciente e à eficácia da substância. Após analisar estudos e documentos, o conselho concluiu não haver evidências científicas que comprovem que os canabinóides sejam totalmente seguros e eficazes no tratamento de casos de epilepsia. Por isso, a prescrição será feita de forma compassiva, ou seja, quando um medicamento novo, ainda não aprovado pela Anvisa, é prescrito exclusivamente para pacientes com doenças graves e sem alternativa terapêutica satisfatória com produtos registrados no país. O usuário terá que assinar um termo de consentimento em que reconhecerá ter sido informado sobre as alternativas de tratamento e os possíveis efeitos colaterais à saúde, que, entre os já identificados, incluem sonolência, fraqueza e alterações do apetite.
“Até o momento, os estudos realizados em humanos têm poucos participantes e não são suficientes para comprovar sua segurança e efetividade. Diante desse quadro, é importante desenvolver urgentemente pesquisas que possam vir a fornecer evidências robustas, de acordo com as normas internacionais de segurança, efetividade e aplicabilidade clínica do CBD”, ressaltou o presidente do CFM, Carlos Vital Tavares Corrêa Lima, esclarecendo que a resolução deverá ser revista em dois anos, quando serão avaliados novos elementos científicos.
Tanto os médicos que receitarem o canabidiol quanto os pacientes que utilizarem a substância deverão ser previamente cadastrados em um sistema informatizado a ser desenvolvido pelos conselhos regionais de medicina. A medida permitirá o monitoramento do uso do produto para avaliar sua segurança e possíveis efeitos colaterais.
Em maio deste ano, a diretoria colegiada da Anvisa colocou em pauta a possibilidade de retirar o canabidiol da relação de substâncias proibidas, inserindo-a na de produtos de uso controlado. A decisão foi adiada pelo pedido de vistas do processo apresentado por um dos diretores da agência.
Dos 297 pedidos de autorização de importação que recebeu até o último dia 3, a Anvisa autorizou 238, 17 esperam o cumprimento de exigências pelos interessados e 34 estão em análise pela área técnica. O prazo médio das liberações é de uma semana.
O uso do CDB passou a ser discutido nacionalmente depois que Katiele Fischer foi a justiça pedindo autorização para usar o medicamento na filha Anny, de 6 anos. Segundo a mãe, Ane tinha até 80 crises convulsivas por semana, e depois que passou a usar o canabidiol esses eventos pararam de acontecer.
Norberto Fischer, pai da menina, diz que a medida é um avanço, mas tímido, já que a resolução, até certo ponto, pode ser considerada restritiva. “Por um lado, ficamos felizes, pois é um avanço o órgão ter se pronunciado sobre o tema, mas a decepção também foi muito grande”, disse Fischer à Agência Brasil. Ele questiona várias decisões, como a de exigir que médicos e pacientes sejam cadastrados no sistema e, principalmente, limitar a cirurgiões e psiquiatras a prescrição do medicamento e estabelecer as doses máximas a serem prescritas.
“Há um excesso de burocracia, como na questão do sistema. Além disso, com base em que o CFM pode estabelecer duas doses no máximo, se ele próprio reconhece não haver parâmetros? Minha filha, por exemplo, toma três doses do remédio por dia. Como o conselho pode dizer que apenas crianças e adolescentes podem se beneficiar do uso do produto?”, pergunta Fischer, lamentando que os usuários do produto não tenham sido ouvidos pelo CFM. “Nenhum pai foi convidado a conversar sobre o teor do texto. Por isso, esperávamos por um avanço, uma resolução corajosa e madura, que desse aos médicos o poder de avançar e salvar vidas. A meu ver, se até aqui alguns poucos médicos se sentiam à vontade para arriscar, eles agora vão se ater ao que está escrito”.
A maconha contém mais de 480 componentes, sendo que 86 são os chamados canabinoides que atuam no cérebro. Os mais estudados são o delta- 9 – tetrahidrocanabinol (THC), que produz efeitos alucinógenos, em doses altas, e o canabidiol (CBD) que não causa efeitos alucinógenos ou psicóticos e protege o cérebro dos efeitos do THC.
iG

Nenhum comentário:
Postar um comentário