A "tortura" de dados para obter resultados favoráveis em estudos sobre
medicamentos novos no mercado é uma prática comum dos laboratórios,
segundo denúncia publicada ontem no "British Medical Journal".
De acordo com o autor, um ex-funcionário de um grande laboratório que
escreveu sob anonimato, os estudos realizados após a aprovação das
drogas têm como objetivo alavancar as vendas dos produtos, e não
determinar sua segurança de uso.
O artigo foi publicado junto com análise de estudos pós-venda de alguns remédios contra diabetes tipo 2.
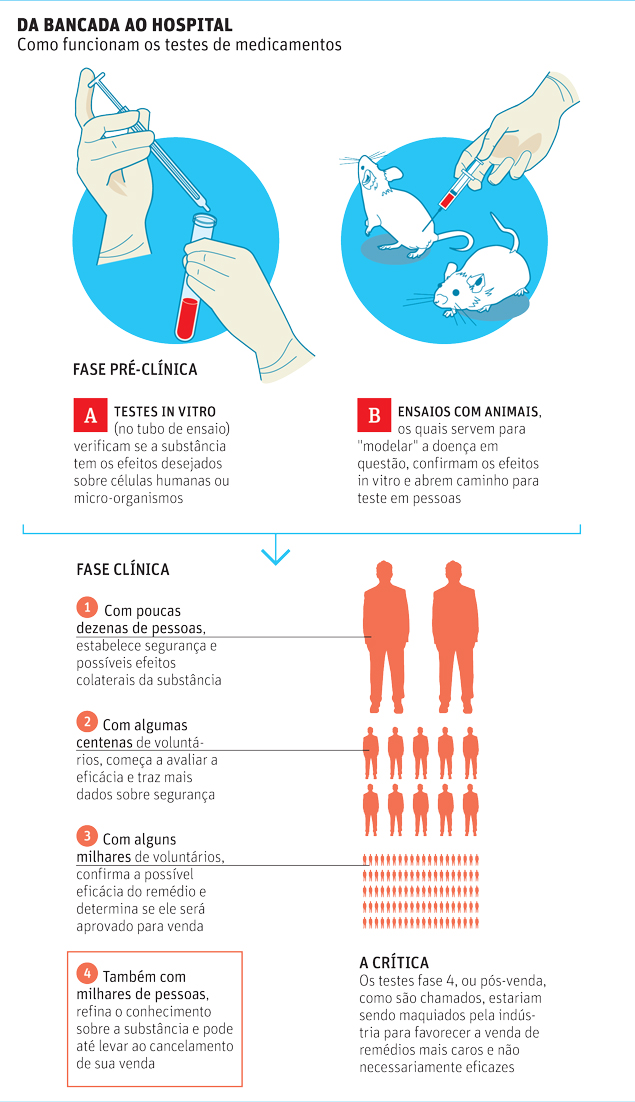
Esse tipo de pesquisa é feito quando a droga está no mercado e,
portanto, já passou pelas três primeiras fases de teste, necessárias
para que o remédio possa ser vendido.
Depois disso, são feitos estudos de fase 4 ou observacionais, que
analisam o desempenho da droga na "vida real", sem as intervenções dos
cientistas e os controles das pesquisas laboratoriais.
| Editoria de arte/folhapress | ||
 |
De acordo com o reumatologista Marcelo Schafranski, autor do livro
"Medicina - Fragilidades de um modelo ainda imperfeito" (Ed. Schoba), a
análise pós-venda é importante para avaliar o peso dos efeitos
colaterais e o custo-benefício das novas drogas.
Mas faltam regras para controlar a metodologia desses trabalhos, muitas
vezes patrocinados e elaborados pelas próprias fabricantes dos remédios.
"Os resultados publicados são escolhidos após a coleta dos dados. São
selecionados desfechos favoráveis para o fabricante do remédio, em vez
de resultados como número de mortes ou internações em UTI. Do jeito que
está, esse tipo de estudo não tem credibilidade."
Segundo a análise feita por Edwin Gale, professor na Universidade de
Bristol, sobre estudos de análogos da insulina conduzidos pelos
laboratórios Novo Nordisk, Eli Lilly e Sanofi, falta rigor científico
nos trabalhos.
Um dos estudos, com mais de 66 mil pessoas, acompanhou os voluntários
por 18 meses (quando o ideal para esse tipo de pesquisa são cinco anos) e
exigia como comprovação de efeito colateral (hipoglicemia) um exame
laboratorial. Com isso, foram registrados pouquíssimos desses eventos,
dando aparência de vantagem da nova droga sobre a antiga.
De acordo com o texto publicado pelo ex-funcionário da indústria, além
de mexer nas estatísticas, os laboratórios permitem que o departamento
de marketing acompanhe todas as etapas dos estudos. O grande número de
pacientes participantes serve, segundo ele, para disseminar a prescrição
do novo remédio entre os médicos.
"Levávamos [médicos] para os melhores hotéis e restaurantes durante as
reuniões. Depois, atuavam como 'embaixadores', dando conferências,
ensinando médicos e falando com a mídia sobre os benefícios da droga."
Outro lado
As empresas citadas nos artigos do "British Medical Journal" responderam por meio de nota aos questionamentos publicados.
O laboratório Sanofi afirmou que acredita que os ensaios clínicos devem
contar com objetivos científicos claros "para ampliar a base de
evidências em prol dos interesses dos pacientes".
Segundo o comunicado, esse princípio é aplicado em todas as pesquisas
conduzidas pela empresa. A Sanofi diz ainda que os estudos atendem aos
quesitos éticos e regulatórios do Brasil.
"No país, foram e são realizados estudos de alto grau de evidência
científica, visando ao melhor controle do paciente com diabetes."
A farmacêutica Eli Lilly afirmou que "não realiza pesquisas médicas com a
intenção de que a condução do estudo aumente as vendas de um
medicamento".
A empresa disse ainda que continua comprometida com a realização de
pesquisas de impacto e relevância, que respondam a questões científicas e
clínicas.
A Novo Nordisk disse que seus estudos clínicos estão "100% alinhados"
com regras estabelecidas pelas agências regulatórias de cada país.
Fonte Folhaonline

Nenhum comentário:
Postar um comentário