 Um levantamento feito pela Interfarma (Associação da Indústria Farmacêutica de Pesquisa) indica que um remédio pode levar até dois anos para conseguir começar a ser vendido no país.
Um levantamento feito pela Interfarma (Associação da Indústria Farmacêutica de Pesquisa) indica que um remédio pode levar até dois anos para conseguir começar a ser vendido no país.
Representantes da indústria farmacêutica reúnem-se hoje com a ministra da Casa Civil, Gleisi Hoffmann, para abordar esses e outros assuntos que podem estar causando um gargalo no mercado.
A burocracia e a quantidade insuficiente de pessoal da Anvisa (Agência Nacional de Vigilância Sanitária), que concede as autorizações, são apontadas como as principais razões para a espera, segundo o monitoramento, feito com base no sistema da própria agência, o Datavisa.
Por meio de sua assessoria, a Anvisa afirmou que esses números não são oficiais. O órgão informou não poder fornecer o tempo de espera dos medicamentos porque usa uma outra maneira de agrupar esses dados.
Dirceu Barbano, diretor-presidente da Anvisa, afirmou, no entanto, que o material apresentado pela Interfarma não é muito diferente das informações da agência.
"Nós não temos dúvidas de que houve um aumento muito grande na demanda, e nós temos um desafio para conseguir absorver tudo isso."
Compatível
"Mas o tempo de espera é compatível com o de outras agências do mundo. É errado e até perigoso dizer que vai faltar medicamento por conta da demora de Anvisa. Poderia causar um temor desnecessário", diz Barbano.
Antônio Britto, presidente da Interfarma, que reúne fabricantes de 80% dos medicamentos de referência no país, criticou a burocracia.
"A Anvisa toma decisões muito importantes para a saúde pública, mas há outras que simplesmente não passam de burocracia", disse.
"A quantidade de funcionários não consegue dar conta de todas as demandas. Mas não basta simplesmente contratar mais gente. Isso precisa de uma mudança de processos, de separar o que é saúde pública da burocracia pura e simples", completou.
Para Antonio Barbosa, presidente do Instituto Brasileiro de Defesa dos Usuários de Medicamentos, a Anvisa deveria estabelecer critérios de prioridade no registro.
"Drogas realmente inovadoras, que vão fazer a diferença para os pacientes, deveriam ter mais prioridade."
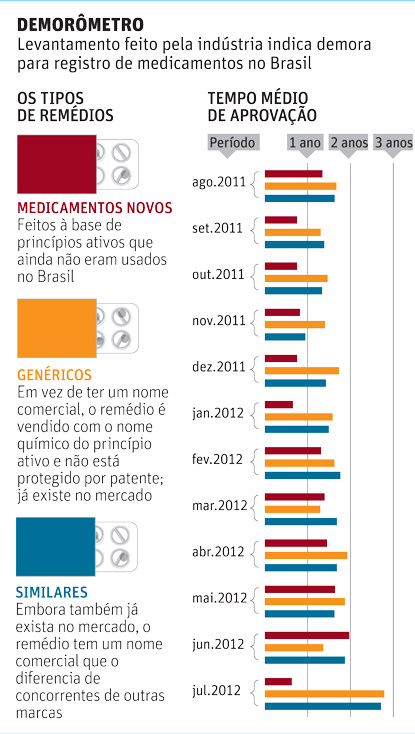
Apelidado de demorômetro, o levantamento da Interfarma foi feito entre agosto de 2011 e de 2012. O tempo médio de espera variou bastante ao longo do período, mas há uma tendência consolidada do aumento da demora.
O problema considerado mais grave foi no caso de novos remédios, em que o tempo de espera passou de sete meses para um ano e quatro meses. Como eles ainda não têm opção de genéricos ou similares, haveria mais chance de deixar pacientes "órfãos".
Mesmo os medicamentos genéricos, que já têm o princípio ativo em uso, também amargam a lista de espera. Segundo o levantamento, nos últimos 12 meses, o tempo médio não foi em nenhuma ocasião inferior a um ano. Medicamentos similares vão pelo mesmo caminho.
O diretor-presidente da Anvisa disse que a agência está trabalhando com afinco para reduzir os prazos, mas que o rigor é fundamental. "É o preço que se paga pelo rigor sanitário. Para proteger a população", afirmou.
Testes clínicos
A lentidão nas autorizações também prejudica os estudos clínicos --pesquisas que avaliam a eficácia de novas drogas-- no país. Várias entidades do setor têm levantamentos semelhantes sobre a situação e, não raro, estudos podem levar mais de oito meses para sair do papel.
"Algumas exigências brasileiras são totalmente descoladas de outras agências de referência no mundo", diz Mariano Janiszewsk, diretor médico da farmacêutia Amgen.
Para Fernando Francisco, da Abracro (Associação Brasileira de Organizações Representativas de Pesquisas Clínicas), o Brasil perde de todos os lados,
"Além de deixar de receber os investimentos, que não são poucos, muitos pacientes acabam sem opção de tratamento. E os profissionais de saúde perdem a oportunidade de ter contato com pesquisas de ponta", diz.
Editoria de arte/folhapress
|
Fonte Folhaonline
|

Nenhum comentário:
Postar um comentário